ALS(筋萎縮性側索硬化症)は運動ニューロンが変性する神経難病です。ALS患者のほとんどは孤発性ですが、約10%程度が家族性に発症するとされ、FUS遺伝子は本邦では2番目に頻度が高いALS原因遺伝子変異です。FUSは主に核に局在するRNA/DNA結合タンパク質で、孤発性ALSの原因タンパク質として着目されるTDP-43と様々な共通項を認めています。ALS-FUS患者の運動ニューロンでは、FUSは細胞質に異所局在し、凝集体を形成します。過去の動物実験等より毒性獲得説が有力とされていますが、その病態機序は未だ不明で治療標的となりうる鍵分子は同定されていません。
本研究ではFUSの新たな結合タンパク質としてDHX30を初めて同定しました (Hikiami R et al., 2022)。DHX30は主にミトコンドリアに局在するRNAヘリカーゼで、ミトコンドリアリボソームの生合成に関与し、ミトコンドリアDNAにコードされるタンパク質の翻訳に重要な機能を有します。さらに遺伝子変異例が神経発達症患者で報告されており、神経細胞において重要な働きを担っていると推察されます。FUS変異体発現培養細胞、ALS-FUS患者の脊髄運動ニューロンでは、DHX30がFUS陽性細胞質内凝集体にリクルートされる事を示しました。さらにDHX30が凝集体形成を促進している可能性が示唆されました。
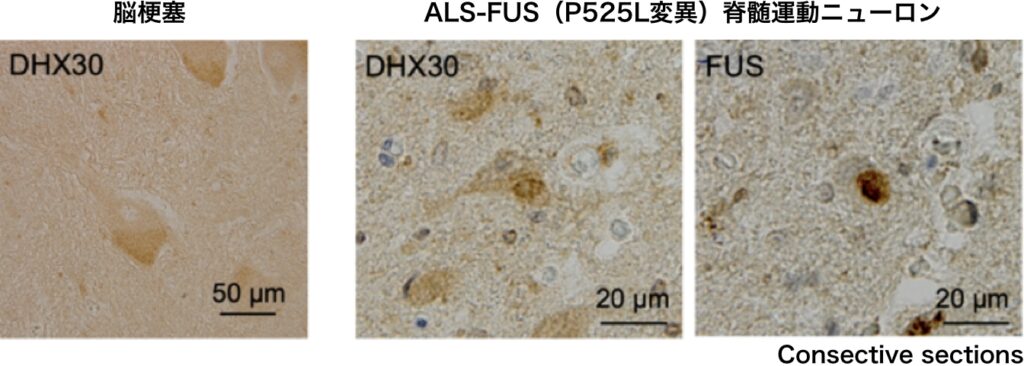
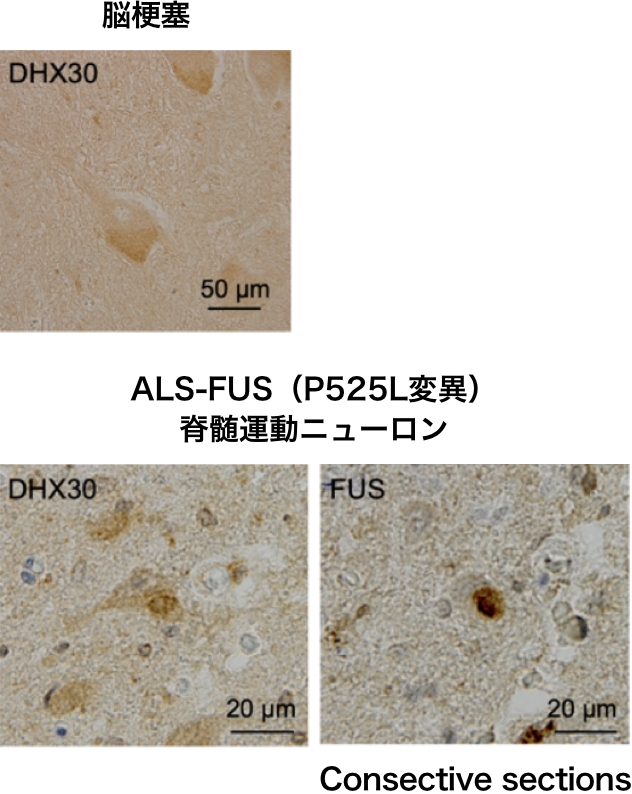
またミトコンドリア内のDHX30は、FUS変異体発現に伴い、SS結合に由来する構造障害を来していました。この構造障害はDHX30の機能喪失につながり、ミトコンドリアタンパク質の合成障害、呼吸鎖複合体の形成障害を介して、神経細胞死を来すことが推察されました。
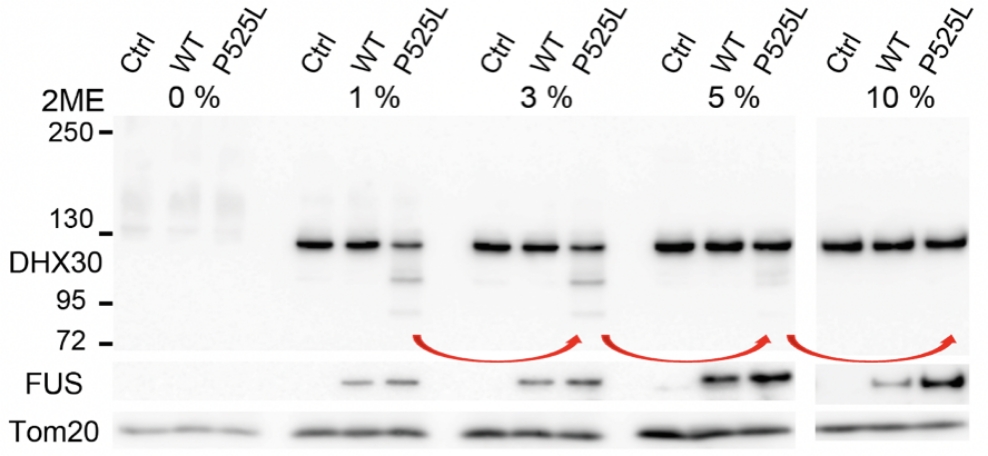
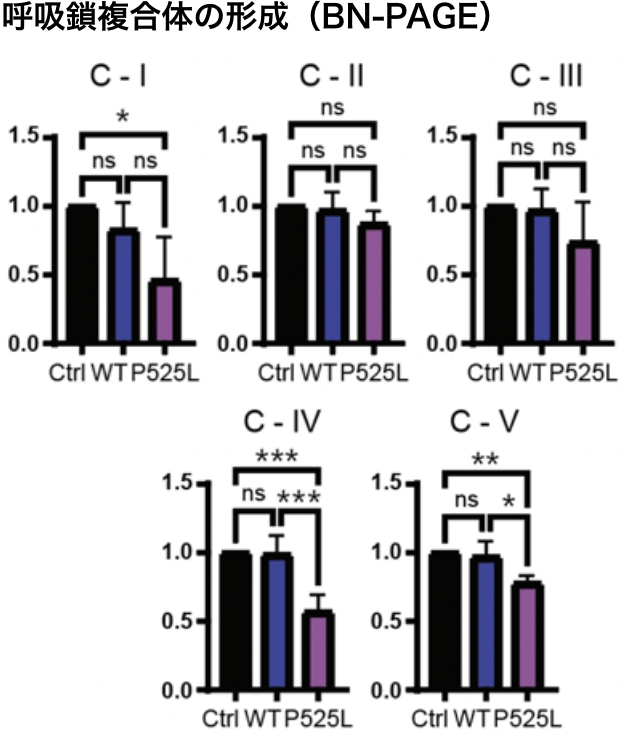
以上よりALS-FUSにおいてDHX30は治療ターゲットとなりうると考え、現在治療法開発に取り組んでいます。
